Entrar
Publicidade
Publicidade
Receba notícias do Congresso em Foco:
Anvisa
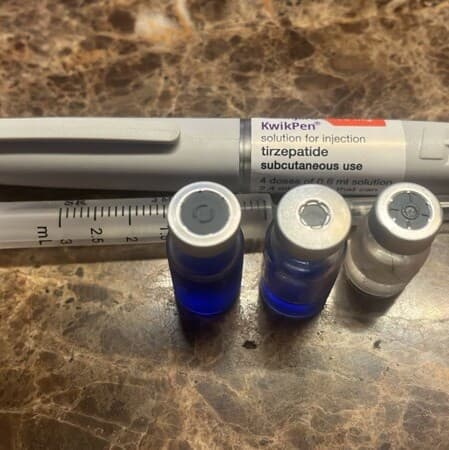
Anvisa anuncia medidas contra canetas emagrecedoras irregulares
Plano prevê revisão de normas, fiscalizações e interdições após alta atípica na importação de insumos.
Congresso em Foco
7/4/2026 18:51
A-A+
A Agência Nacional de Vigilância Sanitária (Anvisa) anunciou nesta segunda-feira (6) um novo pacote de medidas para reforçar a segurança no uso de canetas emagrecedoras diante do avanço de irregularidades na importação de insumos e na manipulação desses produtos. O plano atinge medicamentos à base de semaglutida, tirzepatida e liraglutida.
Entre as ações estão a revisão das regras de manipulação, a intensificação de fiscalizações em farmácias, clínicas e empresas importadoras, além da possibilidade de suspensão de autorizações de funcionamento de estabelecimentos considerados de risco. A agência também vai ampliar a cooperação com vigilâncias sanitárias estaduais e municipais e com órgãos reguladores internacionais.
A decisão foi motivada por um crescimento considerado incompatível na entrada de insumos farmacêuticos ativos (IFAs) usados na produção dessas canetas. Segundo levantamento da Anvisa, mais de 100 quilos de insumos foram importados apenas no segundo semestre de 2025, volume suficiente para a preparação de cerca de 20 milhões de doses.

A decisão foi motivada pela alta atípica na entrada de insumos.Freepik
Em 2026, a agência realizou 11 inspeções em farmácias de manipulação e importadoras, que resultaram em oito interdições por falhas técnicas e ausência de controle de qualidade. Entre os principais problemas identificados estão deficiências de esterilização, falta de rastreabilidade dos insumos, ausência de identificação de origem e produção sem previsão concreta de demanda.
O diretor-presidente da Anvisa, Leandro Safatle, afirmou que o foco das novas medidas é assegurar a qualidade e a eficácia dos medicamentos colocados à disposição dos pacientes. Segundo ele, o controle sanitário precisa garantir que produtos injetáveis tenham padrões rígidos de pureza e esterilidade para evitar riscos à saúde.
O plano de ação foi estruturado em seis eixos, que incluem aprimoramento regulatório, fiscalização, articulação institucional, priorização do registro de novos medicamentos, comunicação com a sociedade e governança interna. Entre os pontos previstos está a busca ativa de eventos adversos em hospitais, emergências e clínicas, com foco em complicações associadas ao uso de produtos manipulados.
Pedidos de registro
A agência informou ainda que existem atualmente oito pedidos em análise para novos medicamentos com semaglutida, mesmo princípio ativo do Ozempic, além de outros nove aguardando início da avaliação técnica.
Apesar de a patente da substância ter expirado no Brasil em março, a Anvisa reforçou que qualquer produto só pode chegar ao mercado após comprovação de segurança, eficácia e qualidade por meio de registro sanitário.
LEIA MAIS
NOTÍCIAS MAIS LIDAS